≪乳がんの治療は「局所治療」と「全身治療」に分ける事が重要≫

乳癌と診断されたら、まず考えるべきことは?

治療が必要となりますが、それにあたり、
重要なことは、「局所 注 1 )」治療と「全身 注 2 )」治療に分けることです。
注 1 ) 「局所」とは「(腫瘍のある)乳腺と(同側の)リンパ節」のこと。
注 2 ) 「全身」とは所謂「遠隔臓器(骨、肺、肝など)」のこと。
〇 局所治療
具体的には手術±放射線のことです。(放射線は「行う場合」と「行わない場合」があるのです)
局所治療1.手術
手術にあたって、重要な観点が以下の二つとなります。
1.乳腺をどうするか?(温存か?全摘か?)
2.リンパ節をどうするか?(センチネルリンパ節生検か? 腋窩郭清か?)
1-1.乳腺をどうするか?
選択肢1.乳腺を部分切除する 乳腺部分切除(温存)+放射線 注 3 )
選択肢2.乳腺を全摘する 乳腺全切除(放射線なし 注 4 ))
注 3 )温存した場合には、(残りの乳腺に)放射線が必須となります。
注 4 ) 全摘した場合には原則として放射線は不要ですが、リンパ節転移が4個以上あった場合には照射適応となります。
その選択(部分切除 or 全切除)は、どうやるの?
それはMRI(拡がり診断)で判断します。
ただ、「乳癌の発生」を意識した安全な部分切除を行わないと「乳房内再発」のリスクが増します。
≪乳癌の発生≫
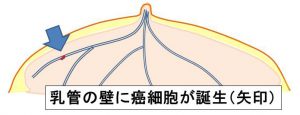
①癌は乳管の壁の細胞が癌化して発生します。
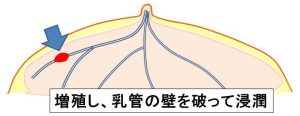
②やがて、増殖し「乳管の壁を破る=浸潤」します。
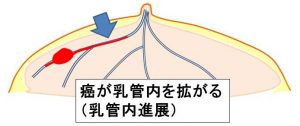
③乳管内を拡がっていきます。(乳頭方向・末梢方向)
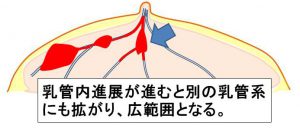
④やがて「別の乳管系」にも拡がり広範囲となる。

上記③までは「温存手術が可能」だけど④になると「温存不能=全摘」となります。

③も温存可能なの? 乳管内の拡がりも大丈夫?

大丈夫だよ。
ただし、きちんと「乳管内の拡がり」を意識した術式 注 5 )にしないと「温存乳房内リスク」が高くなります。
注 5 )当院での温存手術では乳管内の拡がりを意識した温存手術としています。
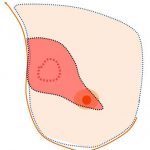
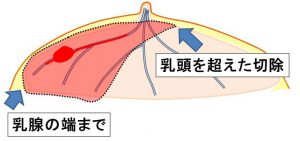
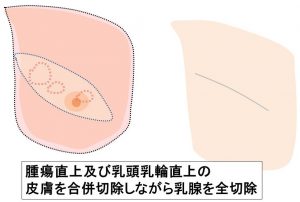
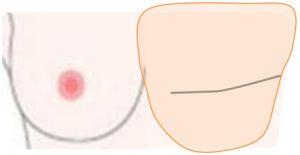
(横から見た図) (正面から) 乳頭乳輪は温存しています。
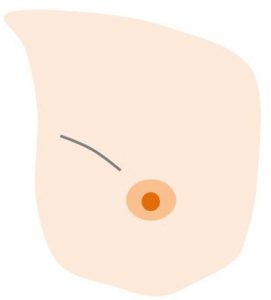
〇実際の傷
あくまでも「乳腺だけ」を「末梢(端)~乳頭を超えて」切除しているのです。
≪温存乳房内再発≫
再発率 10%程度 5%以下
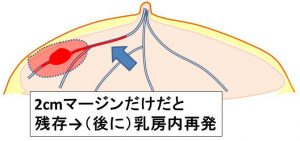

これについては、是非『今週のコラム 204回目 温存手術後の乳房内再発は20%(!)~5%まで幅があると思います。これは手術のやり方なのです。』をご参照ください。
≪全摘の適応≫
全摘の適応は「広範な乳管内進展(左下)」と「全く独立した多発(右下)」となります。

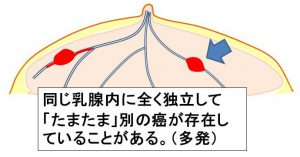
全摘のイメージ
1-2.リンパ節をどうするか?

リンパ節の手術を理解するには、まず「リンパ管の流れ」を理解することが必要です。
≪リンパ管の流れ≫
①癌~センチネルリンパ節
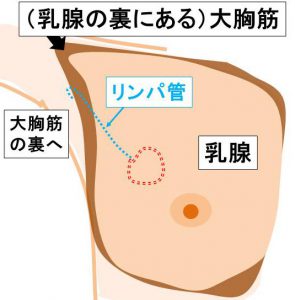
リンパ管のルート
癌から出たリンパ管は乳腺皮下を通り、
大胸筋の外縁を回り込み、大胸筋の裏へ入っていきます。
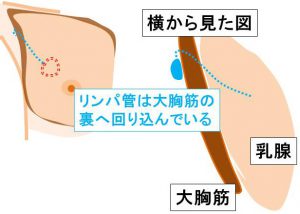
横からみると、位置関係がわかります。
この最初のリンパ節を「センチネルリンパ節 注 6 )」と呼びます。
注 6 )センチネルリンパ節とは「見張りリンパ節」のことで、
「レベル1リンパ節の中で最も、癌に近い部位」と理解してください。(センチネルリンパ節もレベル1リンパ節の一員です)
センチネルリンパ節(大胸筋の裏にある)
乳腺からのリンパ流(青線)は大胸筋の表面を通り、(その外側で)大胸筋裏面を内側へ流れる
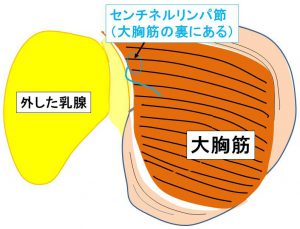
センチネルリンパ節(大胸筋の外縁を内側に引っ張り直視する)
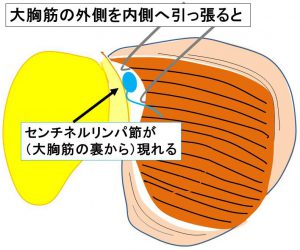
このリンパ節を摘出して、病理医に提出することを
『センチネルリンパ節術中迅速診断』といいます。
②センチネルリンパ節~レベル1
レベル1リンパ節(大胸筋を更に引っ張るとレベル1と小胸筋を直視する)
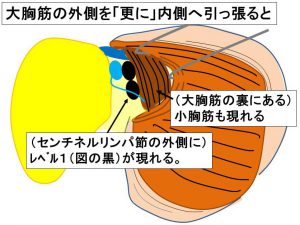
『センチネルリンパ節生検術中迅速診断』で陽性(転移あり)の場合、そのまま腋窩郭清へ移行します。
③レベル1~レベル2リンパ節
小胸筋も一緒に内側へ引っ張ると小胸筋の裏のレベル2を直視する
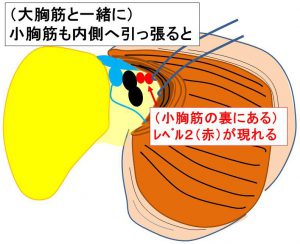
「センチネルリンパ節生検術中迅速診断」で陽性だった場合、
通常、ここまで(レベル2)郭清となります。

ここから先は、殆どの乳腺外科医が経験したことがない世界です。
④レベル2~レベル3リンパ節
小胸筋を外側へ引っ張ることで小胸筋の更に奥にあるレベル3が大胸筋と小胸筋の間の「隙間」から見える。
「隙間」を覗き込むので「視野が悪い」
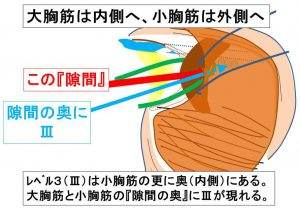
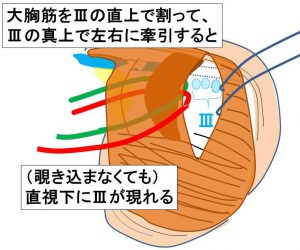
④’レベル3を直視下とする
レベル3を(隙間から覗き込むのではなく)直視下とするために、大胸筋も(レベル3直上で)割る。
リンパ節の位置については
『今週のコラム 179回目 乳癌診療の基本Ⅱ vol.3 大胸筋の『裏側』にリンパ節が外側→内側へ向かって、レベル1→レベル2→レベル3となっていることがご理解いただけましたか』も、是非ご参考にしてください。
≪(リンパ節の)実際の術式の適応(選択)≫
①センチネルリンパ節生検
適応:術前「画像診断」にて転移性のリンパ節を認めない場合に行う
上記、センチネルリンパ節だけを術中に取りだし、術中迅速病理診断 注 7 )を行い、
陰性であれば⇒それ(センチネルリンパ節)だけで終了
陽性だった場合には⇒(通常)レベル2まで郭清 注 8 )
注 7 )術中にセンチネルリンパ節をとりだし、そのまま(術中に)病理医による診断(迅速診断)を得る
ここで注意が必要なのが、「術中の病理医による、その場での診断」という点です。
つまり、その施設に「常勤の病理医がいない」場合にはこの術式が「そもそも」不可能となります。(そのような施設は、まだまだ存在します)
注 8 )通常と書きましたが「センチネルリンパ節生検で陽性だった場合」には施設によって対応が若干異なります。
⇒『今週のコラム 163回目 乳癌診療の基本2 腋窩リンパ節の取り扱い 「そりゃ、もう大騒ぎさ 」』をご参照ください。
②(センチネルリンパ節生検をせずに)最初から郭清を行う場合
適応:術前「画僧診断」にて転移性のリンパ節を認めた場合に行う
レベル1(センチネルリンパ節も含む)に転移所見所見がある場合 ⇒ レベル2まで郭清
レベル2やレベル3にも転移所見がある場合 ⇒ レベル3まで郭清 注 8 )
注 8 )レベル3郭清(鎖骨下郭清ともいう)は手技的に難易度が高く、かつリスクを伴うので避けられがち。

どうして?

≪リンパ管の流れ≫の図④及びず④’の操作(小胸筋を外側へ牽引する)が実は(慣れないと)かなり「大変」かつ「危険」なのです。
小胸筋を外側へ引っ張るためには、小胸筋裏面にあるリンパ節を血管(腋窩静脈)」から(視野の悪いなか)剥がさなくてはならない。 (この操作は一歩間違うと腋窩静脈からの大出血に繋がる)
更に、レベル3を剥がすこと自体、(視野の悪い中)やはりこの血管からの出血のリスクがあるからです。
それで『レベル2まで郭清して、レベル3は放射線で済ませてしまおう』という乳腺外科医が多くなってしまったのです。
その背景については以下のコラムをご参照ください。
『今週のコラム 82回目 この小胸筋を(大胸筋から)剥がして、外側へ引っ張りだす操作が(視野が悪い事もあり)結構慣れが必要なのです。』
『今週のコラム 177回目 乳癌診療の基本Ⅱ vol.1 予後も一緒。郭清範囲も一緒ならば術前化学療法をゴリ押しする理由が解らないわ!』
局所治療2.放射線
2-1.温存乳房照射
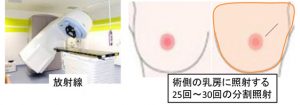
手術で「温存手術(部分切除)」を選択した場合には残りの乳腺に照射します。
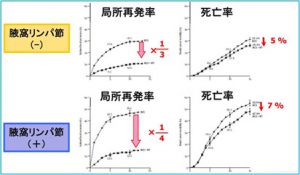
これにより温存乳房内再発のリスクは1/3となります。

そもそも、温存手術は「術後温存乳房照射を前提」とした術式なのです。
例外(温存しても、照射を省略する場合)
●ご高齢(90歳以上はいいでしょう)
●病変が十分以上に狭い範囲なのに、かなりのマージンがある場合(数値化できないので、あくまでも主観です)
2-2.全摘後の胸壁及び鎖骨上照射
リンパ節転移が4個以上の場合が適応となります。

それと、T4症例ですね。
もともと皮膚症状が強くて(術前抗がん剤などで縮小して)手術した場合、やはり「局所再発(皮膚)」が心配となります。
2-3. 再発の場合の適応
・骨転移への照射
「疼痛」もしくは「骨折」の原因となっている場合
ターゲットがはっきりしている場合(単発でコントロールされているなど)
・その他の部位への照射
鎖骨上や頸部、縦隔リンパ節など(他に遠隔転移が無い場合など、積極的に照射してもよい)
肝、肺など tomotherapy 注 9 )であれば、全身療法の補助的に有効です。
⇒このケースでは、「あくまでも全身療法でコントロールされていること」が絶対条件です。
注 9 )tomotherapyは小型のリニアックを360°螺旋状に回転させ(照射したくない部位を避けながら)照射したい部位をピンポイントに狙うIMRT(Intensity Modulated Radiation Therapy)です。
また、IGRT(Image Guided Radiation Therapy)により位置補正を行う高精度の治療
☆重要臓器(大血管や心臓など)の傍にある標的(転移リンパ節など)を狙うのに最適です。
〇 全身治療
全身治療とは内服(消化管で吸収されてから血管に入る)や点滴(直接、血管に入れる)で、投与されます。
再発治療とは異なり「目に見える全身の病巣は無い」わけですが、
『目に見えていないだけで(いずれ可視化するかもしれない)身体のどこかに潜んでいるかもしれない病巣』
⇒放っておけば再発に繋がる、これらに対する治療が「全身治療」という概念なのです。
全身治療(薬物療法) 総論
『術後補助療法(再発予防)なのか、再発治療なのか?』。
薬物療法を語る上で、上記の区別はとても大事です。
☆薬剤にとって、再発治療として適応承認されるのは容易だが、「術後補助療法として適応承認されるには、さらなる壁がある」のです。
「乳癌で使用される薬剤(全体)」
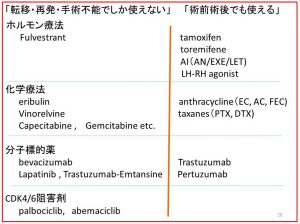
表の右の薬剤は「術前術後でも適応有」薬剤であり、
術後補助療法(再発予防)の場合には、ここからの選択となります。
1-1.全身治療(薬物療法)vol. 1 術後補助療法
「術後補助療法(再発予防)で使える薬剤」

ホルモン療法(閉経前と閉経後に分けられる)
化学療法(anthracycline とtaxaneのみです)
分子標的薬(trastuzumabとpertuzumabのみです)

薬物療法を考えるうえで重要なポイントは
1.適応のある薬剤(上記)
2.サブタイプはどうなのか?
薬物療法は「subtype(サブタイプ)注 10 )」によって決まるという理解が重要です。
注 10 )subtype(サブタイプ)とは、腫瘍の性格のことです。
≪サブタイプについて≫
具体的にはER, PgR, HER2で免疫染色を行い、まず以下に分けます。
1.ルミナールタイプ(ER陽性)
2.HER2タイプ(ER陰性かつHER2陽性)
3.tripple negative(TN)
ルミナールタイプは更に「細分化」されます。
まずHER2も陽性だと ルミナールB(HER2陽性):俗に言うtripple positive
HER2陰性のものは(更に)Ki67の免疫染色により
Ki67低値:ルミナールA
Ki67高値:ルミナールB
☆Ki67が中間値(20~40)の場合にはOncotypeDXで(AなのかBなのか)決定します。
結果として以下の5通りに分けられます。
1-1.ルミナールA
1-2.ルミナールB(HER2陰性)
1-3.ルミナールB(HER2陽性)
2. HER2タイプ
3. TN

まずは、あなたのサブタイプが上記(5通りのうちの)どれなのか?
それが大事です。 (by 大事マンブラザーズバンド)
≪術後補助療法(の実際)≫
1-1.ルミナールA ⇒ホルモン療法(閉経前、更年期:tamoxifen, 閉経後aromatase inhibitor)
1-2.ルミナールB(HER2陰性) ⇒抗がん剤(TC 注 11 ))+ホルモン療法(上記)
1-3.ルミナールB(HER2陽性) ⇒抗HER2療法 注 12 )+ホルモン療法(上記)
2. HER2タイプ ⇒抗HER2療法
3. TN ⇒抗がん剤(anthracycline+taxane 注 4 ))
TC 注 11)
⇒T(docetaxel)+C(cyclophosphamide) を4回投与(非anthracycline regimen)
抗HER2療法 注 12 )
⇒ trastuzumab(ハーセプチン:分子標的薬)+抗癌剤
trastuzumabは1年間投与、それに抗がん剤を組み合わせる。
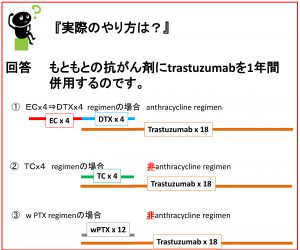
ECだけはtrastuzumabとは同時併用していないことに注意してください。
E(anthracycline)もtrastuzumabどちらも心毒性があるため
♯ Eによる心毒性は不可逆性(生涯投与量が決まっている)
trastuzumabによる心毒性は可逆性(何回でも使用可)

これにpertuzumabも併用できるって聞いたけど、それはどんな時?
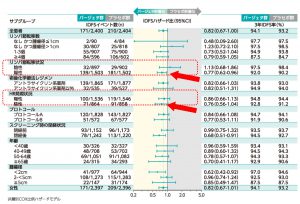
⇒ まずは、pertuzumabが術後補助療法として承認されたAPHINITY試験を示します。
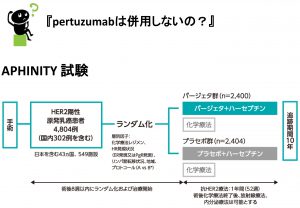

APHINITYのsubgroup解析を参考にして
日本での適応が左記のようになってます。

pertuzumabについては、(日本では)若干適応があいまいなのですが…
「リンパ節転移陽性」もしくは「再発リスクが高い」症例
⇒この後者の解釈は…
「腫瘍径が大きい」「ER陰性」「グレード高」などが(一般的に)言われています。
anthracycline+taxane 注 13 )
⇒ 乳癌のKey drugであるanthracyclineとtaxaneを両方とも行う「最強レジメン」です。
●anthracycline系薬剤
E(Epirubicine)とA(Adriamycin)があります。
心毒性はEの方が抑えられているため、生涯投与量がE(900mg/m2) , A(500mg/m2)となっています。
♯これ以上投与すると不可逆的な心毒性を引き起こす
単独では使用されることなく、C(cyclophosphamide)やF(5Fu)と併用されるため歴史的に
FEC, FAC, EC, ACなどとして用いられます。
●taxane系薬剤
術後補助療法として用いられるのはdocetaxel(DTX)とpaclitaxel(PTX)となります。
臨床試験の結果DTXは3週に1回のregimen、PTXは毎週投与のregimen(weekly PTX:wPTXと略)として用いられます。
◎実際のanthracycline + taxane レジメン
(個人的に)最も一般的と思うのは ECx4 ⇒ DTXx4
他に ECx4⇒wPTXx12 ACx4⇒DTXx4 ACx4⇒wPTXx12, FECx4⇒DTXx4など「あらゆる」組み合わせが可能です。

治療がサブタイプによって決まることは解ったけど、例外は無いの?

ルミナールAでは「ホルモン療法単独」と書いたけど、いまだに『リンパ節転移があるのに抗がん剤しなくてもいいの?』という考え方が根強いと感じます。
これについては、下記に挙げたコラムをまずはお読みください
『今週のコラム 188回目 このデータを見ても、まだ「リンパ節転移があると(ルミナールAでも)化学療法が必要だと思いますか??」』
『今週のコラム 189回目 「リンパ節転移があれば抗がん剤をすべき」という古い考えが完全否定される日も近いのです。』

結局どういうことよ?

RxPONDER試験の結果でリンパ節転移1-3個ではOncotypeDXの結果の信頼性が確定します。
言い換えれば「リンパ節転移(1-3個)のルミナールAでは抗がん剤は不要(上乗せ無)」
ということだよ。

逆に言うと、ルミナールAでもリンパ節転移4個以上なら抗がん剤が必要なの?

そこが、難しいところ。
「リンパ節転移4個以上でも、ルミナールAなら抗がん剤は無意味」という証明が(現時点で)無い以上、
抗がん剤を勧めない理由がないのです。
もしもこのケース(リンパ節転移4個以上のルミナールA)で抗がん剤をする場合はanthracycline + taxaneになるかな?
♯ リンパ節転移4個以上で非anthracyclineレジメンであるTCの有効性が証明されていない限り、スタンダードはanthracycline+taxaneとなるのです。
1-2.全身治療(薬物療法)vol. 2 再発治療
まずは以前掲載した表でみると、

今回は(この表の)左右共に使える。
つまり「何でもアリ」となります。

治療戦略は「2ステップ」となります。
それでは詳細を見ていきましょう。
第1ステップ まずは「画像上CR clinical CR」を目指す。
「遠隔転移(再発)に根治はない」と言われていますが…
過去にも数パーセント存在したし、「薬物療法が進歩した現在」では実際にどの程度なのか?
誰にも正確なことは言えません 注 1 )
注 1 ) 実際に江戸川で診ている(再発)患者さんの中にも「長期間CR:complete responseを継続(つまり異常所見が無いということ)」している患者さんは結構いらっしゃいます。
○転移(再発)状況(臓器など)による戦略

転移臓器によって治療法(戦略)が異なるってことなの?

その通り、我々乳腺外科医がよく使う言葉に「life threatening(生命を脅かす)」があります。
つまり転移は「life threatening」と「non life threatening」に分けて考える 注 2 )のです。
ザックリ分けると
注 2 )脳転移は薬剤が届かないので(基本的には)局所治療(放射線)となるので、ここでは除きます。
life threatening
①肝転移(小さいものは除く)
②多発性(でかつ)大きな肺転移
③癌性胸膜炎で呼吸症状を伴うもの
non life threatening
①骨転移
②リンパ節転移
③単発の肺転移や(病巣の小さな)多発肺転移、小さな肝転移
○治療の実際
1.life threateningに対する治療

一言でいうと…
「ガツンと叩く」
(サブタイプ別に)
1-1.HER2陽性
⇒抗HER2療法(trastuzumab + pertuzumab + 抗がん剤)となります。
・抗がん剤の選択としては(術前術後に用いていないtaxane=another taxane 注 3 ))もしくはeribulin
注 3 )術前術後でdocetaxelを用いていれば、paclitaxelを用いるし、(逆に)paclitaxel既治療ならばdocetaxelの事
・(術前術後にanthracyclineを用いていなければ)anthracyclineを用いてもよい。
1-2.ルミナールタイプ
⇒(通常の)抗がん剤
・これも術前術後に用いていないものを優先
例)術前術後にanthracycline + taxaneならばanother taxaneとなるし
術前術後にTCならば、まずは(第1選択)anthracycline、その後(第2選択)paclitaxelとなります。
another taxaneとしてpaclitaxelとなる場合には
⇒(単独よりも)より効果を狙ってbevacizumab+paclitaxelとすることも多い
1-3.トリプルネガティブ
(かつては)
⇒通常は術前術後にanthracycline + taxane既治療なので、必然的にanother taxane , eribulinなどとなります。
やはりpaclitaxelの場合にはbevacizumab併用とすることも多い。
でしたが…
(現在は)まず BRACAnalysisとPD-L1抗体の検索を行ってから戦略を立てることになります。
・BRACAnalysisが陽性ならばOlaparib 注 4 )PD-L1陽性ならばatezolizumab + nab-paclitaxelが適応となります。
これらの順番については、「病状(転移の状況」「既治療歴(抗がん剤の)」などにより決まりはありません。
注 4 )Olaparibの添付文章に「アントラサイクリン系抗悪性腫瘍剤及びタキサン系抗悪性腫瘍剤を含む化学療法歴のある患者を対象とすること」と明記されています。
2.non life threateningに対する治療
2-1.HER2陽性
⇒life threateningの場合と同様、抗HER2療法を行います。
この場合は最初trastuzumab+pertuzumab+抗がん剤
⇒(その後)抗がん剤を抜いて「trastuzumab + pertuzumabのみ」とする戦略へ移行します。
2-2.ルミナールタイプ
⇒(かつては)ホルモン療法変更(のみ)とすることも多かったですが、
CD4/6inhibitor(palbociclib/abemaciclib)の登場で一変しました。
まずはpalbociclib(abemaciclib)+Fulvestrant(閉経前なら、更にLH-RHagonist併用)が第1選択となります。
◎BRACAnalysisが陽性の場合にはOlaparib⇒上記治療となることが多い
2-3.トリプルネガティブ
⇒non life threateningであっても「抗がん剤」しか治療がないので、life threateningと治療は同様となります。
第2ステップ (第1ステップで得られた)画像上CR(そうでなければ可能な限りCRに近い)状態を維持する。
第1ステップでは(副作用よりも)効果を優先しての治療ですが、ここ(維持)は『忍容性のある治療を如何に継続させるか』」が優先されます。
ルミナールタイプの場合にはpalbociclib + Fulvestrant ⇒ (最終的に)ホルモン療法単独
HER2の場合にはtrastuzumab+pertuzumab(分子標的薬)のみ
TNの場合は抗がん剤しないと無治療となるため、長期間の「低用量」抗がん剤⇒(最終的に)無治療

再発治療戦略について解説しました。
よく『一生、抗がん剤止められないよ。』みたいに言う医師がいますが…
現実に(副作用のある)抗がん剤を一生継続することは不可能です。
大事な視点は「抗がん剤を使わない(使わなくても安心な)状態」を作り、それを維持する。
前者が第1ステップであり、後者が第2ステップなのです。
第2ステップが待っていると思えば(それなりに辛い)第1ステップも頑張れるのです。