漸く手に入りました。
まだデビュー前。 いい顔してます。
○ 術前抗がん剤の重要な事実
1.本来の適応(役割)
(そのままでは)大きすぎて温存手術不能なので「小さくして温存したい」場合に行う
注意:全ての腫瘍が「小さくなれば温存できる」タイプとは限りません。
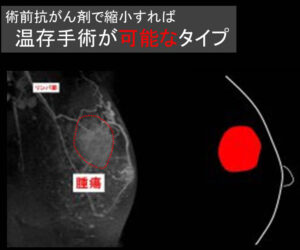
温存可能なタイプ
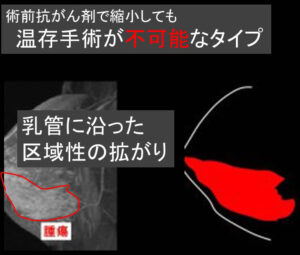
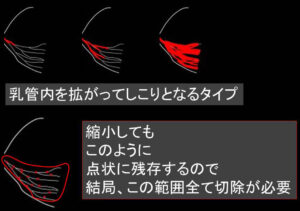
温存不可能なタイプ
2.抗癌剤は術前に行っても術後に行っても予後は変わらない
所謂、「再発」治療の場合には「全ての」抗癌剤の使用が可能(適応がある)であるが、「術前術後、つまり再発予防目的」の場合には使える抗癌剤が限定されています。
anthracycline と taxaneのみ
まず、このことの理解が必要です。
♯HER2 陽性の際の分子標的薬 trastuzumab, pertuzumabも「術前術後に」使えます。
以下の2つの症例を提示します。
どう思いますか?
症例1.術前抗がん剤後に手術を行ったことが局所再発を招いたのでは?と考える症例
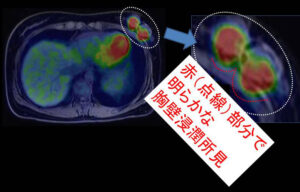
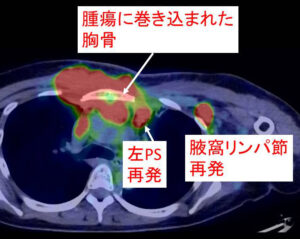
左乳癌の部分ですが、
明らかに胸壁浸潤があります。
NAC後に乳房全摘+センチネルリンパ節生検されています。
初診時に胸壁浸潤してはいたが(画像上)リンパ節転移所見が無かったためセンチネルリンパ節生検をして(結果)陰性であったので郭清が省略されています。
しかし、比較的早期にそれは起こりました。
明らかな局所再発(胸壁及びPS,Ax)
注)PS:parasternum node傍胸骨リンパ節
Ax:axillar node腋窩リンパ節
○問題と感じている事。
もしも術前抗がん剤せずに手術していたら、当然腫瘍が浸潤している部分(腫瘍床)の大胸筋も手術で摘出したはずです。
♯何故なら、胸壁浸潤といっても胸筋を切除すれば取り切れる可能性は高いからです。肋骨への直接浸潤は普通はありません。
それが、(術前抗がん剤で)肉眼的には大胸筋から外れたため腫瘍床部の大胸筋にmicro levelで癌細胞が残存したため(早期の)局所再発をしたと考えられます。
また、腋窩リンパ節にも再発していることはセンチネルリンパ節生検自体が術前抗がん剤により不正確になった。(再発した腋窩リンパ節は本来センチネルリンパ節と認識されるべきだったのだが、別のリンパ節をセンチネルリンパ節と認識されてしまったため生じた腋窩再発と言えます。
ここで術前抗がん剤が持つリスクは
1.術前抗がん剤することにより、本来切除されなくてはいけない部分(術前抗がん剤により癌が消えたように見えるが顕微鏡レベルでは癌細胞が残存している部分)が取り残されてしまうリスク
⇒結果、局所再発(胸壁)
2.術前抗癌によりセンチネルリンパ節生検が正しく行われないリスク(真のセンチネルリンパ節が認識されなかったために転移したリンパ節が見逃されてしまった)
⇒結果、局所再発(腋窩リンパ節)

結果として
単に、「術者が楽をするための」術前抗がん剤であったとも言えます。
症例2
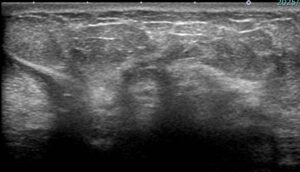
エコー像
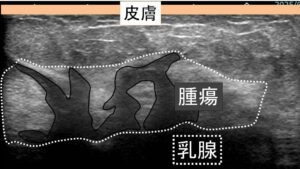
上記を解説するとこれになります。
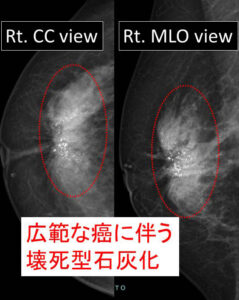
腫瘍は乳腺内に「歪な」拡がりがあります。
初診時のクリニックの針生検では非浸潤性乳管癌
大病院へ転院
術前抗がん剤「一択」の提示
えっ? 非浸潤癌なのに術前抗がん剤?
おかしいと思うでしょ?
どうやら、その大病院の医師は「どうせ、こんなに広範囲なのだから、どこかに浸潤しているに違いない」と考えたのでは?
幾ら何でも(万が一広範囲だとしても)微小浸潤とか「5mm以内」(勿論、浸潤無もありえる)結果として抗癌剤の適応が無い症例に(術前)抗癌剤をすることになってしまう。
↑
術前抗がん剤を(もしも、この患者さんが担当医に押されて行ったとしたら)結局そもそも最初の浸潤径がどうだったのか?全く解らなくなる
そうすると、例えば(術前抗がん剤後の)手術標本で「非浸潤癌のみ残存」という病理結果が出たとしても(例え、実際には「そもそも最初から非浸潤癌だけだった」としても)担当医は『抗癌剤が効いたから非浸潤癌しか残存しなかった』と適当に言えるし、それを『最初から非浸潤癌だかだったかもしれないでしょ!』と反論してもその証拠がないのです。
普通に考えて「そもそも」(術前にしろ術後にしろ)抗癌剤が不要かもしれないのに、そして「患者さん自身が希望していないのに」何故、そうも術前抗がん剤をゴリ押しするのか?
そこには(以前、掲示板にも挙げましたが)2つの臨床試験(前者がTN、後者がHER2 type)をよく知ることが必要です。
その上で、本当に自分にとって術前抗がん剤は必要だ!と思えるのであれば、その時こそ(その患者さんにとっては)正しいと言えるのだと思います。
KERNOTE-522があります。
本来「転移再発」にしか適応がない免疫チェックポイント阻害剤である「pembrolizumabを術前抗がん剤としてなら使える(だからpembrolizumabを使うために術前抗がん剤が正義だ)」とした、かなりトリッキーなものですがそれを根拠に「術前抗がん剤はトリプルネガティブでは最早標準!」と思っているようです。
HER2陽性に対するKATHERIN試験もどうかと思いますが(まだ、HER2陽性にはanti-HER2 therapyが効きやすいというある種の安心感があるのに対し)私が口酸っぱく言っているように「トリプルネガティブは単一集団ではなく、抗癌剤が効かないものも当然ある」という認識なしでは手術不能という事態を招き得るのです。 手術不能となると「抗癌剤も効かないし、手術もできない」となります。
術前抗がん剤の安全神話など存在しません
実際に、術前抗がん剤が効かなかった時誰が責任をもてるのか?
QA管理番号12660を回答していて、そのリスクについて真剣に考えましょう。
これら「術前抗がん剤をゴリ押しすることの正当化?」の根拠とされている2つの臨床試験を詳細します。
KEYNOTE 522
術前化学療法群と術前pembrolizumab+化学療法+術後pembrolizumab(9 cycles)の比較
対象 2期以上 2期75%, 3期は25%
T2 68%
N0 50% N1 40%
アジア人 21-23%
結果
pCR率 pem群 64.8% vs 51.2% プラセボ群
5y EFS pem群 81.2% vs 72.7% プラセボ群
5y OS pem群 86.6% vs 81.7% プラセボ群

この2つの臨床試験だけで
「トリプルネガティブにもHER2陽性にも術前抗がん剤しなくてはいけない」という根拠になっているのです。
しかし、これらの臨床試験をしっかり理解しなくてはいけません。
当たり前のことですが、臨床試験は(その薬剤を開発した)製薬会社が、その薬剤の売り上げを伸ばすために行っていることは常に頭に入れておかなくてはなりません。
KEYNOTE 522
まず1期が含まれていないことを確認してください。
⇒1期の可能性があるのに「トリプルネガティブ=術前抗がん剤」としてゴリ押しするとしたら、それの根拠にはなりません。
2期が75% 3期が25%含まれていることを意識しつつ成績を見ると有意差のある結果と言えます。
⇒但し、ここで2つの問題点を指摘しておきます。
問題点1 トリプルネガティブとは「単一の」集団ではなく、ER, PgR,HER2 が陰性であるだけの雑多な集団であること
当然ながら「抗癌剤が効きやすい」ものも含まれているし、逆に「抗癌剤が全く効かない」ものも含まれている、無論その「中間」も含まれています。
⇒ここで問題となるのは「ギリギリ現時点で手術可能な症例で術前抗がん剤を選択する」ことにより「もしも抗癌剤が全く効かないタイプであれば、手術不能に追い込まれる(しかも手術もできない。薬も効かないということが何を意味するのか?」
担当医はそうなった場合の責任を持てるのか?
担当医はこのように言い訳するかもしれない。『抗癌剤が効かなかったということは、手術先行しても、術後の抗癌剤が効かないってことだから(そもそも)再発必発だったんだよ。』
⇒一見、正しそう?に聞こえますが手術先行した症例が全て再発するわけではない。つまり「手術だけで(たとえ抗癌剤が効きにくいいタイプだとしても)再発しない」症例は必ず存在するわけです。
手術不能一歩手前を手術先行した経験が(他医師よりも間違いなく多い)私の経験から断言します。
問題点2 immune-related adverse events: irAEの存在
術前に行えば(本来、転移再発乳癌にしか適応がない)pembrolizumabが使える!
これを根拠としているわけですが、
有害事象としての免疫チェックポイント阻害剤特異的なirAEをどう考えるか?
pembrolizumabの添付文章
間質性肺炎
大腸炎、下痢
肝機能障害
腎機能障害
内分泌障害 副腎不全
通常の術前術後に適応のある抗がん剤(anthracycline, taxane)の副作用は使用経験が長く対処方法、薬剤が豊富に対して、それ以上の有害事象を抱える可能性がある。
転移再発のように「現にここに再発している癌に対して必要なのだから許容せざるを得ない」ということと
術前術後のように「使わなくても再発しない可能性があるのに、敢えて使用することで無駄に有害事象で苦しく可能性」
この理解が重要なのです。

以上を理解したうえで私が、このpembrolizumabを用いた術前化学療法を使うべき(又は、使ってもよい)と考える対象として思い浮かぶのは
比較的若く、勉強熱心で上記を全て理解したうえで
『irAEのリスクも承知しています。トリプルネガティブだからといって抗癌剤自体も効かないタイプなのかもしれないことも承知しています。ただとにかく1%でも生き続ける可能性にかけたいんです。』という患者さんです。
無論、上記であっても「手術不能となるリスクが高い状態」とか(逆に)早期の場合には決して選択してはいけない。
また、患者さん自身が化学療法先行(もしくは化学療法自体に抵抗があるのに)ゴリ押しなどとんでもない!
KATHERINE
術前anti-HER2 therapyでpCRとならなかった症例をtrastuzumab群とT-DM1群で比較
対象 HER2陽性早期乳癌患者を対象♯1
注意点1 実際は進行例が25%を占めている
♯1 「早期」と銘打っておきながら実際の対象は
手術不能 T4/NX/M0 or TXN2-3/M0 25%
手術可能 T1-3/N0-1/M0 75%
注意点2 アジア人は僅か8.7%
結果
7年無浸潤疾患生存 T-DM1 80.8% vs 67.1% trastuzumab
7年生存率 T-DM1 89.1% vs 84.4% trastuzumab
ここで浸潤性疾患とは
同側の浸潤性乳癌の再発
同側の局所領域の浸潤性乳癌の再発
遠隔再発
対側の浸潤性乳癌
問題点1 「早期」と銘打っていながら「手術不能が25%含まれている」こと
当然ながら「早期は再発率が(そもそも)低く、進行すればするほど再発率は高い」わけだから、この「25%含まれている手術不能症例」が、数値を引っ張っている可能性がある。
やはり対象を「早期」と銘打っていながら「4期以外の全ての症例を対象とした数値」なのだから、実際には早期患者さんに使うべきではないのでは?
問題点2 そもそも比較が「T-DM1 vs trastuzumab」であること
通常はtrasuzumab+pertuzumab (phesgo)を用いることが多いので単純に比較はできない。
問題点3 術後にT-DM1(14回 つまり9か月)かなりつらいのでは?
術前に抗癌剤+分子標的薬 3か月ないし半年は許容できても更に「術後に抗癌剤9か月」が患者さんのQOLを確実に損なう

トリプルネガティブとは異なり「anti-HER2 therapyに効果が高い筈の」集団なので「効かない場合には手術不能に追い込まれる」リスクは、トリプルネガティブよりは低いとはいえ、やはり「手術不能ギリギリの状態」に勧めるのはリスクがある。
本当に早期では(そもそも)差が「かなり少ない」可能性は十分にある。
なので対象は(手術不能でないが、それなりに進行=3期のイメージ)で、更に術後も9か月抗癌剤をモチベーションを持って出来る「心身ともに健康な」人
当然、高齢者に勧めるべきではない。